La corrosione è processo naturale e irreversibile che determina una consumazione lenta e continua di un metallo con conseguente peggioramento delle caratteristiche o proprietà fisiche del materiale coinvolto. È fondamentale proteggere le superfici metalliche in modo che questo fenomeno non diminuisca la funzionalità dei manufatti, ma al tempo stesso anche per non generare gravi danni economici e rischi per la sicurezza.
La corrosione è un fenomeno di deterioramento lento e continuo di un materiale metallico causato dall’ossidazione delle superfici. Le cause che portano all’ossidazione e alla conseguente corrosione del metallo sono molteplici, tuttavia le forme più comuni riguardano l’attacco da parte di agenti atmosferici o di liquidi, detti corrosivi, che entrano in contatto con la superficie metallica.
L'Organizzazione internazionale per la normazione ha infatti definito, all’interno della norma UNI EN ISO 8044, il fenomeno della corrosione come l’interazione chimica-fisica tra un metallo e il suo ambiente, che causa cambiamenti nelle proprietà del metallo e che può determinare un deterioramento significativo della funzione del metallo, dell’ambiente o la riduzione dell’efficienza del sistema tecnico di cui questi fanno parte.
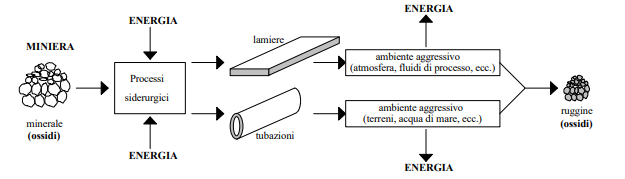
Sostanzialmente, la corrosione è la tendenza dei corpi metallici a trasformarsi nel tempo perdendo la proprietà originali, cioè a deteriorarsi e ritornare spontaneamente allo stato in cui si trovano in natura che è quello di combinazione con altri elementi, in particolare con l'ossigeno, dal quale erano stati sollevati nei processi metallurgici mediante somministrazione di energia (elettrica, chimica o di calore). Per questo motivo, la corrosione è anche chiamata antimetallurgia.
Sebbene il fenomeno della corrosione possa colpire differenti materiali, come sottolinea la normativa sopracitata, esso è spesso associato ai supporti metallici, ovvero ai metalli e alle loro leghe – anche a quelli che sono naturalmente dotati di uno strato passivante. In particolare, il fenomeno della corrosione colpisce acciaio al carbonio, inox e leghe di alluminio trasformati in lamiere, estrusi e profilati.
Come si sviluppa la corrosione?
Per dar vita a questo fenomeno sono quindi necessari due elementi:
- processi di natura elettrochimica a cui prendano parte il materiale metallico (elettrodo);
- l’ambiente di corrosione (elettrolita).
Gran parte dei metalli si presenta in natura con una forma stabile. Per raggiungere la propria stabilità con meno energia, un atomo di metallo perde uno o più elettroni dalla propria struttura. Questi combinandosi con altri elementi come ossigeno, zolfo o cloro presenti nell’ambiente, fanno si che il metallo si ossida.
Ambienti e meccanismi di corrosione
A seconda dell'ambiente in cui ha luogo la corrosione, essa può essere classificata in:
- Corrosione in ambiente secco
La corrosione secca non si verifica in presenza di acqua o umidità, ma quando il metallo entra in contatto con alcune sostanze – tra cui l’anidride solforosa, l’idrogeno solforato, acido solforico, ecc. - che danno origine a fenomeni di ossidazione.
Nel caso più comune, la sostanza che si lega al materiale metallico provocando la sua ossidazione è l’ossigeno.
La corrosione secca si verifica sempre a temperature elevate.
La corrosione in ambiente umido avviene in presenza di acqua, ossigeno, elementi di natura chimica (piogge acide, detergenti, secrezioni di insetti, ecc.) o di natura fisica (temperatura, sollecitazioni meccaniche, ecc.).
I fattori che più influenzano la corrosione variano nelle diverse zone climatiche, nelle zone rurali, industriali e marine. L’azione di sostanze chimiche aggressive presenti in atmosfera in combinazione con elevata umidità può generare un rapido degrado del metallo a causa del sottile film liquido che funge da elettrolita ed in base alle sue peculiarità può influenzare fortemente l’entità della corrosione. Il film tende a formarsi quando l’ambiente raggiunge una soglia di umidità critica.
Per classificare il comportamento della corrosione dei materiali che operano nelle diverse località si fa riferimento a quattro ambienti:
- ambiente rurale: località lontane da scarichi e zone costiere.
- ambiente urbano: località residenziali o commerciali con inquinamento contenuto.
- ambiente industriale: presenza di industrie pesanti (chimiche/metallurgiche).
- ambiente marino: luoghi vicino alle coste.
- Ulteriori forme di corrosione
Forme di corrosione fisica meccanica sono causate da sollecitazioni di natura elettrochimica e meccanica, indotte sul manufatto o interne ad esse: corrosione per sfregamento, corrosione per fatica, tensocorrosione.
Inoltre, vi sono anche fenomeni di corrosione di natura biologica che derivano dal contatto del materiale metallico con acque o suoli biologicamente attivi.
Morfologia dei fenomeni di corrosione
La superficie di tali metalli può essere colpita da:
Corrosione generalizzata
Come suggerisce il nome stesso, questa tipologia di corrosione interessa l’intera superficie di un oggetto metallico e si traduce in un assottigliamento dello stesso. Possiamo distinguere tra:
- corrosione uniforme quando il fenomeno colpisce l’intera superficie e la gravità degli effetti corrosivi è uguale in qualsiasi punto;
- corrosione disuniforme quando invece la corrosione interessa tutta la superficie del materiale, ma l'entità degli effetti corrosivi è più o meno evidenziata in punti differenti.

Corrosione localizzata o pitting
Il termine corrosione localizzata viene utilizzato quando il fenomeno interessa soltanto specifici punti della superficie. Questa forma di corrosione si presenta come attacchi localizzati, denominati anche pit o vaiolature, le cui dimensioni variano da poche decine di micron ad alcuni millimetri. La zona colpita può presentare diverse morfologie, tra cui ulcere, crateri, punte di spilli, bordi di grano, ecc.
Questa forma di corrosione è considerata più pericolosa rispetto a quella generalizzata, poiché è meno visibile a occhio nudo.

Corrosione selettiva
La corrosione selettiva indica il fenomeno che causa la dissoluzione preferenziale di un costituente del materiale metallico che è più facilmente attaccabile per ragioni chimiche o metallografiche. Essa interessa soprattutto le leghe metalliche e consiste nella dissoluzione preferenziale del metallo meno nobile per esposizione ad ambienti di media corrosività; il metallo più nobile, che non risulta aggredito, rimane allo stato metallico in forma di residuo poroso. Tra gli esempi più comuni rientrano la cosiddetta dezincificazione degli ottoni e la grattificazione delle ghise.
Proteggere i metalli dalla corrosione
I metalli vengono utilizzati per produrre edifici, infrastrutture, automobili, tantissimi altri oggetti che ci circondano. E sebbene il deterioramento del metallo dovuto alla corrosione è un fenomeno naturale, essa non è gradita. Ecco perché è importante proteggere le superfici metalliche adeguatamente. Innanzitutto, è bene ricordare che alcuni metalli, tra cui i materiali più nobili dell’acciaio, come ad esempio argento, rame, piombo, nichel e cromo, o non hanno bisogno di essere protetti in quanto non subiscono il processo di corrosione o vengono verniciati per migliorare l’aspetto estetico di un manufatto. Al contrario, l’acciaio necessita di essere protetto mediante protezione di tipo attivo o passivo.
La protezione passiva evita il contatto con il metallo applicando uno strato sottile impermeabile che è in grado di isolare la superficie del metallo stesso dagli agenti aggressivi e/o con l’aggiunta di composti chimici adeguati, tra cui rivestimenti organici (vernici) e rivestimenti metallici (zinco, nichel, cromo). La protezione di tipo attivo, denominata anche catodica, impedisce invece la formazione di corrosione trasformando tutti i punti anodici sulla superficie metallica in punti catodici, erogando corrente elettrica.
Un problema economico
Se finora ci siamo occupati della corrosione da un punto di vista tecnico, non dobbiamo dimenticare che questo fenomeno rappresenta anche un problema economico. Ogni anno infatti i danni provocati dalla corrosione – relativi all’ambiente, persone e cose - sono valutati in milioni di euro e si stima che circa un quinto della produzione annuale di acciaio è destinato alla sostituzione di parti danneggiate dalla corrosione.
Un cartello esposto in uno stand della NACE-CORROSION del 2002, il principale incontro del settore che ogni anno si tiene in una città degli USA, citava: “Mentre tu leggi questo cartello si corrodono 30.000 Kg di ferro”, il che sottolinea quanto il fenomeno della corrosione sia ampiamente diffuso.
Oltre a ridurre la funzionalità di un materiale, la corrosione è un fenomeno che va contrastato in quanto può avere ripercussioni negative sia in termini ambientali – pensiamo ad esempio a gasdotti, oleodotti e piattaforme che potrebbero originare disastri ecologici – sia in termini di sicurezza nel caso in cui a essere colpiti fossero sistemi di fissaggio o parti strutturali di ponti, treni e aerei, il cui cedimento dovuto alla corrosione potrebbe avere conseguenze drammatiche.
 Ponte Morandi. © Il Sole 24 Ore
Ponte Morandi. © Il Sole 24 OreProteggere adeguatamente i materiali metallici dalla corrosione è dunque essenziale. Sebbene ciò possa comportare una spesa anticipata elevata, una corretta ed efficace protezione anticorrosiva contribuisce a risparmiare denaro e risorse a lungo termine.
Un caso esemplare: la Tour Eiffel
Il monumento più famoso di Francia, costruito da Gustave Eiffel in occasione dell’Exposition Universelle del 1889 con l’obiettivo commemorare il centenario della rivoluzione francese, è costituito da ferro con una bassa percentuale di carbonio.
Ogni 7 anni, la Tour Eiffel viene completamente riverniciata per proteggere il metallo dalla formazione di ruggine e dalla corrosione causata dall’inquinamento atmosferico e dagli escrementi degli uccelli. Questa operazione richiede ogni volta circa 14 mesi, 25 operai, 50 tonnellate di vernici e costi elevatissimi, che potrebbe però essere stati inferiori. Secondo uno studio di un esperto tedesco infatti, se la Tour Eiffel fosse stata zincata a caldo, gli interventi di manutenzione avrebbero avuto una cadenza di 17 anni con un risparmio di oltre 10 milioni di dollari.
Inoltre, durante l’ultima operazione di restauro iniziata nel maggio 2019, gli operatori si resero conto che i 19 strati derivanti dalle operazioni di manutenzione precedenti presentavano profonde crepe in diversi punti, tanto da rendere impossibile l'adesione di un nuovo strato di vernice. Questa operazione implica la raschiatura degli strati precedenti sul 10% della struttura, l’eliminazione di circa 30 tonnellate di vernice precedentemente utilizzata e l’applicazione di 60 tonnellate di nuovo prodotto verniciante. Il costo di tale operazione – che terminerà nell’anno in corso – è di oltre 40 milioni di euro.
